05 May De un sueño de infancia al Premio Israel: La trayectoria de Shulamit Michaeli en la ciencia del ARN
Shulamit Michaeli recibe el Premio Israel 2026 en ciencias biológicas por su investigación pionera sobre el ARN de parásitos; su trabajo ha contribuido a una mejor comprensión de las enfermedades infecciosas y podría dar lugar a nuevos tratamientos.
Por Maayan Eilon Ashkenazy/Instituto de Ciencias Davidson

Prof. Shulamit Michaeli (Foto: Bar-Ilan University)
La profesora Shulamit Michaeli recibió el Premio Israel 2026 de Investigación en Ciencias de la Vida. El galardón le fue otorgado el 78º Día de la Independencia, en reconocimiento a sus contribuciones al estudio del ARN de patógenos causantes de enfermedades infecciosas. «Es muy emocionante», declaró Michaeli en una entrevista con el Instituto Davidson.
Profesora de microbiología en la Universidad Bar-Ilan, Michaeli es pionera en la investigación del ácido ribonucleico (ARN) de parásitos. Su trabajo se centra en parásitos que causan enfermedades graves, como la leishmaniasis cutánea, provocada por el parásito Leishmania. Durante muchos años, ha estudiado cómo estos parásitos infectan a sus huéspedes y se comunican, con la esperanza de desarrollar un tratamiento eficaz.
Michaeli obtuvo su licenciatura con honores en la Universidad de Tel Aviv. «Siempre me atrajeron las ciencias biológicas, especialmente su intersección con la química», comentó. «Fui una de las primeras estudiantes en acceder directamente al programa de doctorado en la Universidad de Tel Aviv». Durante sus estudios de doctorado, investigó la actividad genética en bacterias, pero al finalizar su doctorado deseaba trabajar con organismos más complejos que las bacterias.
«Justo en ese momento, la biología molecular comenzaba a tomar forma, junto con el estudio de enfermedades que la ciencia y la medicina habían ignorado en gran medida hasta entonces, a pesar de que afectan a millones de personas». El organismo que eligió fue un parásito unicelular. «Fue un sistema ideal para mí», afirmó, «porque me introdujo tanto en el mundo de los parásitos como al de una importante enfermedad infecciosa».
Michaeli realizó su trabajo postdoctoral en la Universidad de San Francisco, donde se introdujo en el campo de la investigación del ARN: moléculas involucradas en numerosos procesos dentro de la célula, especialmente en la ejecución de las instrucciones codificadas en el ADN y su traducción a las proteínas que produce la célula. Durante este tiempo, participó en el descubrimiento de un proceso conocido como trans-empalme, en el que las moléculas de ARN de un parásito se cortan y se vuelven a unir para permitir la producción de proteínas específicas.
En 1990, Michaeli estableció su propio laboratorio en el Instituto Weizmann de Ciencias. En aquel entonces, según cuenta, el ARN parasitario «no se consideraba un tema de gran interés, y la gente no comprendía realmente su importancia. Pensaban que lo más importante era el ADN, por ser el material hereditario en sí mismo, y las proteínas, porque son las que realizan el trabajo propiamente dicho. El ARN se veía simplemente como un intermediario. Pero yo comprendí su importancia y me dediqué a él durante toda mi vida profesional».
Un pequeño cambio puede alterar por completo la estructura del ribosoma de un parásito. El parásito Leishmania experimenta cambios durante su ciclo de vida al pasar del flebótomo a un huésped mamífero.
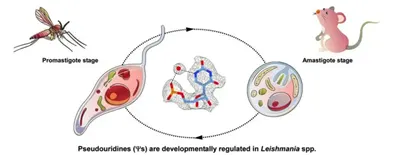
Un pequeño cambio puede alterar por completo la estructura del ribosoma de un parásito. El parásito Leishmania experimenta cambios durante su ciclo de vida al pasar del flebótomo a un huésped mamífero (Rajan, K. S. et al. Cell Reports (2024)).
Un nuevo comienzo
En 1998, Michaeli se trasladó a la Universidad Bar-Ilan. «Comencé una nueva vida y, afortunadamente, tuve mucho éxito», comentó. Incluso después de la mudanza, mantuvo una estrecha relación con sus colegas del Instituto Weizmann y continúa colaborando con investigadores de allí. En un estudio que publicó recientemente con la premio Nobel Ada Yonath, del Instituto Weizmann de Ciencias, quien descifró la estructura del ribosoma — la maquinaria celular de síntesis de proteínas — ambas descubrieron que el ribosoma del parásito Leishmania se adapta a los cambios en su entorno.
El parásito se desplaza desde el intestino de la mosca de la arena hembra hasta el torrente sanguíneo del mamífero al que pica. Esta transición implica un cambio importante de temperatura, de unos 27 grados Celsius en el intestino de la mosca a unos 37 grados en el cuerpo del mamífero. Para sobrevivir en su nuevo entorno, el parásito debe adaptarse, y lo hace mediante cambios químicos únicos en sus ribosomas. Michaeli y Yonath demostraron que incluso un solo cambio de este tipo puede alterar la estructura completa del ribosoma y, por consiguiente, la variedad de proteínas que puede producir. «Fuimos de los primeros en demostrar que estas adaptaciones cambian a medida que el parásito transita entre sus dos etapas de vida, y que esto es lo que permite que sus ribosomas funcionen a temperaturas tan diferentes», afirmó Michaeli.
Michaeli también descubrió un mecanismo único mediante el cual se silencian las moléculas de ARN dentro de los núcleos de los parásitos tripanosoma, causantes de la enfermedad del sueño, y de los parásitos leishmania. Conocido como interferencia de ARN, o ARNi, este mecanismo involucra una clase específica de pequeñas moléculas de ARN. Estas moléculas se unen al ARN mensajero, que transporta las instrucciones de codificación de proteínas del ADN al ribosoma, e impiden la producción de ciertas proteínas cuando no son necesarias. «Durante mi carrera, fui de los primeros en argumentar que el ARNi existe no solo en el citoplasma celular, sino también en el núcleo mismo, y lo llamamos snoARNi» – una forma de interferencia de ARN pequeño que se encuentra en el nucléolo, una estructura dentro del núcleo celular.
Más recientemente, Michaeli descubrió un mecanismo distintivo de respuesta al estrés basado en este proceso: cuando las condiciones se vuelven desfavorables, el parásito puede desencadenar su propia muerte. Lo hace interrumpiendo la producción de moléculas de ARN mensajero, que contienen las instrucciones necesarias para producir las proteínas esenciales para su supervivencia y funcionamiento. Para lograrlo, el parásito detiene la maquinaria de empalme de ARN, lo que activa un proceso de autodestrucción. Michaeli también descubrió que ciertos fármacos pueden activar este mecanismo de autodestrucción y ahora trabaja para comprender cómo el parásito lleva a cabo esta autodestrucción y qué moléculas están involucradas.
La molécula que Michaeli y sus colegas descubrieron induce al parásito a un estado de latencia.
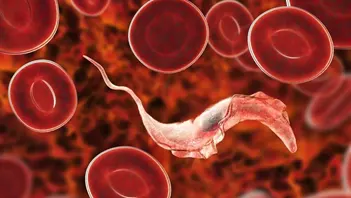
La molécula que Michaeli y sus colegas descubrieron induce un estado de latencia en el parásito. Ilustración de un parásito tripanosoma en el torrente sanguíneo (Ilustración: Kateryna Kon/ Shutterstock).
Hablando el idioma de los parásitos
Michaeli descubrió recientemente un tipo de molécula de ARN largo, conocida como lncRNA, que determina cuándo un parásito tripanosoma se transforma en la forma que le permite infectar a los humanos. Esta molécula también permite que los parásitos se muevan juntos en grupo. Esta capacidad es esencial, ya que los parásitos deben viajar desde el intestino de la mosca tse-tsé (Glossina) hasta sus glándulas salivales, desde donde se transmiten a los humanos a través de una picadura. El estudio demostró que, cuando falta esta molécula, los parásitos ya no pueden moverse juntos, lo que impide la propagación de la enfermedad. Fue el primer estudio en definir el papel de este tipo de ARN en el ciclo reproductivo del parásito.
También descubrió que los parásitos se transmiten información entre sí mediante exosomas – pequeñas vesículas que contienen ARN y proteínas que secretan para alertarse mutuamente del estrés. «Intento comprender su lenguaje y cómo se comunican entre sí», explicó Michaeli. «Demostramos que, si se encuentran en mal estado, secretan exosomas que les indican a los demás parásitos: “No nos lleven en el largo viaje; no estamos bien”. Todavía estoy intentando comprender qué componentes de los exosomas transmiten ese mensaje».
En otro estudio, Michaeli y sus colegas identificaron una molécula de ARN exclusiva del parásito. «Tenemos un estudio asombroso, en colaboración con un grupo de Portugal, que demuestra que una sola molécula pequeña de ARN nucleolar puede hacer que el parásito de la enfermedad del sueño deje de infectar», afirmó Michaeli. La molécula que descubrieron, también un tipo de ARN largo no codificante (lncRNA), contiene una pequeña molécula de ARN cuya función es inhibir la actividad de las moléculas de ARN mensajero implicadas en el desarrollo del parásito.
Cuando el parásito infecta a una persona, se multiplica rápidamente en el torrente sanguíneo y causa una enfermedad grave. Sin embargo, en cierta etapa, deja de reproducirse para completar su ciclo de vida, permaneciendo en la sangre del paciente hasta que otra mosca pica al individuo e ingiere la sangre rica en parásitos. Resulta que esta molécula recién descubierta es la responsable de inducir al parásito a un estado latente. Por lo tanto, aumentar la producción de la molécula puede forzar a los parásitos a entrar en este estado de latencia. En este estado, son incapaces de reproducirse y la infección activa en el huésped mamífero se detiene. «Actualmente continuamos con esta investigación y pronto publicaremos un artículo innovador sobre el tema», concluye.
Sin bajar el ritmo
Michaeli afirma que su laboratorio está desarrollando un tratamiento para la leishmaniasis cutánea basado en una nano-partícula que penetra en la célula del parásito y la destruye en veinte minutos. El tratamiento ya ha mostrado resultados prometedores en estudios con animales, y su equipo colabora ahora con el Centro Médico Tel Aviv Sourasky para adaptarlo a uso humano. El siguiente paso serán los ensayos clínicos para comprobar su seguridad y eficacia en personas. De tener éxito, podría suponer un cambio significativo para las comunidades afectadas por la leishmaniasis cutánea en Oriente Medio, África, Asia y Latinoamérica.
«Hoy, mirando hacia atrás, puedo decir que mi contribución a largo plazo para descifrar las singulares vías de la biología del ARN en los parásitos tripanosomas está siendo reconocida», declara Michaeli. «Por ejemplo, la comprensión de que el ARN puede modificarse después de su producción surgió de estudios sobre tripanosomas».
La gente me pregunta: «Shula, ya has recibido el Premio Israel, ¿quizás sea hora de bajar un poco el ritmo?». “Pero nunca trabajé por un premio. Trabajé porque amo lo que hago. Incluso cuando enseño a estudiantes y jóvenes investigadores, es importante para mí transmitirles ese amor por la microbiología y el ARN. He contribuido a formar a toda una generación de investigadores de ARN en Israel.”
Ganar el premio no la ha frenado. Al contrario, su pasión por el trabajo sigue creciendo. «Tengo becas de investigación y un laboratorio lleno de estudiantes, y siento que apenas estoy empezando. Mi amor por este campo se profundiza con el tiempo, porque la tecnología actual permite hacer cosas tan extraordinarias que es imposible parar. Es un momento excepcionalmente emocionante para la ciencia».
- Contenido distribuido por el Instituto Davidson de Educación Científica
Traducción: Consulado General H. de Israel en Guayaquil
Fuente: YnetNews