18 Ene Cáncer de próstata, novedosa droga israelí ya está aprobada en México

Una gran noticia respecto al cáncer de próstata Un ensayo clínico de fase III ha concluido con éxito en América Latina, con la participación de 80 pacientes, que confirmaron la alta tasa de mejorías locales y efectos secundarios mínimos, como lo demuestran las biopsias y el seguimiento de los pacientes.
Una terapia inventada en el Instituto Weizmann de Ciencia y clínicamente desarrollada en colaboración con Steba Biotech (Luxemburgo) ha sido aprobada por la Cofepris, autoridad de salud de México, para el tratamiento focal de cáncer de próstata en etapa temprana.
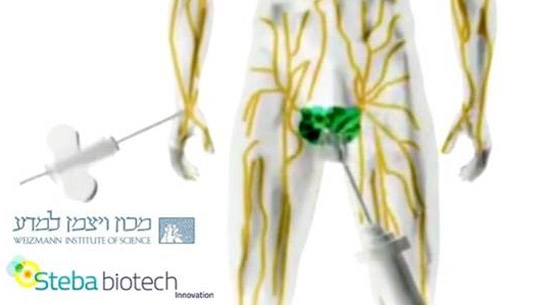
La terapia consiste en un láser y un fármaco novedoso, TOOKAD® Soluble.
Un ensayo clínico de fase III fue realizado en México, Perú y Panamá, con la participación de 80 pacientes, confirmando los buenos resultados ya reportados en ensayos clínicos de fase II, como se evidencia por las biopsias negativas y el mantenimiento en los pacientes en términos de potencia, continencia y la calidad de vida en general.
La aprobación de comercialización en México viene a raíz de la reciente finalización de un segundo ensayo clínico de fase III en Europa.
Este estudio de progresión de la enfermedad en comparación al azar, la tasa libre de cáncer se midieron junto con las funciones urinarias y de erección en pacientes tratados con TOOKAD® soluble y sometidos a vigilancia activa en un seguimiento de dos años.
Cáncer de próstata y pruebas exitosas
Para esto se involucró a más de 400 pacientes en 43 hospitales de 11 países europeos y se encuentra actualmente en proceso de evaluación por la Agencia Europea de Medicamentos (EMA).
La terapia aprobada sigue un nuevo paradigma desarrollado por el Profesor Yoram Salomon del Departamento de Regulación Biológica y el Profesor Avigdor Scherz del Departamento de Ciencias del Medio Ambiente en el marco de la terapia fotodinámica.
Se compone de una infusión intravenosa de TOOKAD® soluble, seguido inmediatamente por iluminación láser de infrarrojo cercano a través de fibras ópticas delgadas que se insertan en el tejido prostático con cáncer, bajo control ecográfico.
Tookad® Soluble fue sintetizado por primera vez en el laboratorio Scherz de bacterioclorofila, el pigmento fotosintético de ciertas bacterias acuáticas que obtienen su suministro de energía de la luz solar.
El fármaco permanece en la circulación sanguínea del paciente hasta que se despeja totalmente 3-4 horas más tarde, y no muestra ninguna toxicidad.
La iluminación confinada del tejido enfermo activa la droga que circula a nivel local, lo que resulta en la extensa generación de moléculas tóxicas de corta duración: el oxígeno y los radicales de óxido nítrico.
Estas moléculas altamente reactivas inician la oclusión rápida y la destrucción del tumor.
Los vasos sanguíneos, provocan la muerte necrótica de todo el tumor sin afectar las estructuras cercanas y sus funciones.
El uso de iluminación de infrarrojo cercano, junto con el rápido aclaramiento del fármaco desde el cuerpo y el mecanismo no térmico de acción único, hacen posible tratar con seguridad tejidos grandes, profundamente incrustados cancerosos utilizando un procedimiento mínimamente invasivo.
La aprobación de comercialización reciente fue proporcionada tanto a la droga (TOOKAD® soluble) como al dispositivo de iluminación láser.
Para ver el video hacer clic en el link https://youtu.be/ydQn5AF9C0k
En el entorno de la terapia focal actualmente aprobada, TOOKAD® Soluble VTP (TS-VTP) es un procedimiento de una duración aproximada de 90 minutos.
Los pacientes son liberados unas horas más tarde y pueden regresar a sus actividades normales dentro de unos pocos días.
Sin ninguno de los efectos secundarios frecuentemente asociados con la extracción de la próstata con cirugía o radioterapia.
Esta nueva tecnología es invasiva mínimamente y ofrece una buena alternativa a los pacientes diagnosticados con cáncer de próstata en etapa temprana.
El número de estos pacientes ha aumentado dramáticamente en las últimas dos décadas debido a la revisión generalizada basándose en los niveles de antígeno específico de la próstata (PSA).
Esta población se enfrenta al dilema de someterse al tratamiento radical de la extirpación de la próstata con el riesgo de una alta morbilidad, o permanecer bajo vigilancia activa con mayor riesgo de progresión del cáncer.
El Instituto Weizmann y Steba Biotech están actualmente llevando a cabo un amplio programa de investigación oncológica en colaboración con varios grupos clínicos en el Memorial Sloan Kettering Cancer Center en Nueva York. Los estudios clínicos acerca del Four cáncer de próstata más avanzado y otras indicaciones oncológicas derivadas de esta investigación están programadas para comenzar en 2016.
Fuente: Latam Israel